21/05/2022
Reakcje utleniania-redukcji, znane również jako reakcje redoks, stanowią fundament wielu procesów chemicznych zachodzących w naszym otoczeniu i w organizmach żywych. Od korozji metali, przez spalanie paliw, aż po oddychanie komórkowe – reakcje redoks odgrywają kluczową rolę. Zrozumienie i umiejętność bilansowania tych reakcji jest niezbędne dla każdego, kto chce zgłębić tajniki chemii.

- Czym są reakcje utleniania-redukcji?
- Dlaczego bilansujemy reakcje redoks?
- Metody bilansowania reakcji redoks
- Kroki bilansowania reakcji redoks metodą stopni utlenienia
- Kroki bilansowania reakcji redoks metodą jonowo-elektronową
- Przykłady zbilansowanych reakcji redoks
- Częste błędy przy bilansowaniu reakcji redoks
- Znaczenie bilansowania reakcji redoks w praktyce
- Najczęściej zadawane pytania (FAQ)
- Podsumowanie
Czym są reakcje utleniania-redukcji?
U podstaw reakcji redoks leży transfer elektronów pomiędzy reagentami. Mamy tutaj do czynienia z dwoma komplementarnymi procesami:
- Utlenianie: Jest to proces, w którym atom, jon lub cząsteczka traci elektrony. W wyniku utleniania stopień utlenienia atomu wzrasta.
- Redukcja: Jest to proces, w którym atom, jon lub cząsteczka zyskuje elektrony. W wyniku redukcji stopień utlenienia atomu maleje.
Kluczowe jest zrozumienie, że utlenianie i redukcja zawsze zachodzą jednocześnie. Nie może być utleniania bez redukcji i odwrotnie. Substancja, która oddaje elektrony (ulega utlenieniu), nazywana jest reduktorem. Natomiast substancja, która przyjmuje elektrony (ulega redukcji), nazywana jest utleniaczem.
Warto zapamiętać podstawową zasadę: redukcja to przyjmowanie elektronów, a nie oddawanie. Oddawanie elektronów to proces utleniania.
Dlaczego bilansujemy reakcje redoks?
Bilansowanie równań reakcji chemicznych, w tym reakcji redoks, jest fundamentalne dla zachowania praw chemicznych, a w szczególności prawa zachowania masy i ładunku. Prawo zachowania masy mówi, że masa reagentów musi być równa masie produktów. W kontekście reakcji redoks, musimy również uwzględnić prawo zachowania ładunku – suma ładunków po stronie reagentów musi być równa sumie ładunków po stronie produktów.
W reakcjach redoks, bilansowanie ma dodatkowy wymiar – bilans elektronowy. Musimy upewnić się, że liczba elektronów oddanych przez reduktor jest dokładnie równa liczbie elektronów przyjętych przez utleniacz. Tylko wtedy równanie reakcji będzie poprawne i będzie odzwierciedlać rzeczywisty przebieg procesu chemicznego.

Metody bilansowania reakcji redoks
Istnieje kilka metod bilansowania reakcji redoks. Dwie najczęściej stosowane to:
- Metoda stopni utlenienia: Ta metoda opiera się na określeniu stopni utlenienia atomów pierwiastków zmieniających swoje stopnie utlenienia w reakcji. Następnie, na podstawie zmian stopni utlenienia, ustala się współczynniki stechiometryczne.
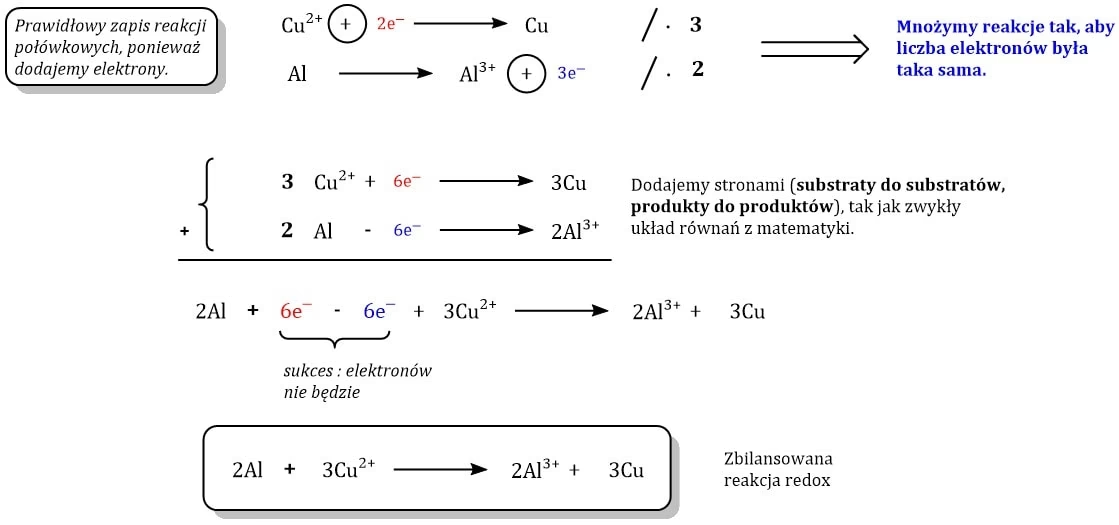
- Metoda jonowo-elektronowa (metoda połówkowych reakcji): Ta metoda polega na rozdzieleniu reakcji redoks na dwie połówkowe reakcje – reakcję utleniania i reakcję redukcji. Każda z tych połówkowych reakcji jest bilansowana osobno pod względem masy i ładunku, a następnie obie reakcje są sumowane w taki sposób, aby elektrony się skróciły.
Obie metody prowadzą do tego samego rezultatu – poprawnie zbilansowanego równania reakcji redoks. Wybór metody zależy często od preferencji i rodzaju reakcji.
Kroki bilansowania reakcji redoks metodą stopni utlenienia
Metoda stopni utlenienia jest często prostsza i szybsza w przypadku reakcji o nieskomplikowanej stechiometrii. Oto kroki, które należy wykonać:
- Zapisz nieskończone równanie reakcji. Zidentyfikuj reagenty i produkty.
- Określ stopnie utlenienia wszystkich atomów w reagentach i produktach. Przypomnij sobie zasady określania stopni utlenienia.
- Zidentyfikuj atomy, które zmieniają swoje stopnie utlenienia. Wskaż, które atomy ulegają utlenieniu, a które redukcji.
- Określ zmianę stopnia utlenienia dla atomów utleniających się i redukujących. Oblicz różnicę w stopniach utlenienia.
- Ustal stosunek liczby oddanych elektronów do liczby przyjętych elektronów. Znajdź najmniejszą wspólną wielokrotność zmian stopni utlenienia i ustal odpowiednie współczynniki.
- Wpisz obliczone współczynniki przed wzorami substancji utleniającej się i redukującej się.
- Dobierz współczynniki stechiometryczne dla pozostałych substancji (jeśli są), bilansując atomy i ładunek. Zaczynaj od atomów, które nie zmieniają stopni utlenienia, często tlenu i wodoru na końcu.
- Sprawdź zbilansowane równanie. Upewnij się, że liczba atomów każdego pierwiastka i ładunek są zbilansowane po obu stronach równania.
Kroki bilansowania reakcji redoks metodą jonowo-elektronową
Metoda jonowo-elektronowa jest szczególnie przydatna w przypadku reakcji zachodzących w roztworach wodnych, zwłaszcza w środowisku kwasowym lub zasadowym. Kroki postępowania są następujące:
- Zapisz nieskończone równanie reakcji w formie jonowej. Rozpisz substancje rozpuszczalne na jony. Substancje nierozpuszczalne, gazy i wodę pozostaw w formie cząsteczkowej.
- Podziel reakcję na dwie połówkowe reakcje: utleniania i redukcji. Zidentyfikuj, które substancje ulegają utlenieniu, a które redukcji.
- Zbilansuj atomy w każdej połówkowej reakcji, z wyjątkiem tlenu i wodoru.
- Zbilansuj atomy tlenu, dodając cząsteczki H2O po stronie, gdzie brakuje tlenu.
- Zbilansuj atomy wodoru, dodając jony H+ (w środowisku kwasowym) lub OH- (w środowisku zasadowym) po stronie, gdzie brakuje wodoru. W środowisku zasadowym, po dodaniu OH-, po obu stronach równania dodaj tyle samo cząsteczek H2O, ile dodałeś OH-, a następnie uprość równanie, skracając cząsteczki wody.
- Zbilansuj ładunek w każdej połówkowej reakcji, dodając elektrony (e-) po odpowiedniej stronie. W reakcji utleniania elektrony pojawią się po stronie produktów, a w reakcji redukcji po stronie reagentów.
- Wyrównaj liczbę elektronów w obu połówkowych reakcjach. Pomnóż każdą połówkową reakcję przez odpowiedni współczynnik, aby liczba elektronów oddanych w reakcji utleniania była równa liczbie elektronów przyjętych w reakcji redukcji.
- Dodaj obie zbilansowane połówkowe reakcje stronami. Elektrony powinny się skrócić.
- Uprość równanie, skracając wspólne cząsteczki (np. H2O, H+, OH-), jeśli występują po obu stronach równania.
- Sprawdź zbilansowane równanie. Upewnij się, że liczba atomów każdego pierwiastka i ładunek są zbilansowane po obu stronach równania.
- Jeśli reakcja zachodziła w środowisku zasadowym i w końcowym równaniu występują jony H+, zneutralizuj je, dodając do obu stron równania tyle samo jonów OH-, ile jest jonów H+. Połącz H+ i OH- w H2O i uprość równanie.
Przykłady zbilansowanych reakcji redoks
Aby lepiej zrozumieć proces bilansowania, przyjrzyjmy się prostemu przykładowi reakcji:
Niezbilansowane równanie: Zn + AgNO3 → Zn(NO3)2 + Ag
Bilansowanie metodą stopni utlenienia:
- Stopnie utlenienia: Zn0 + Ag+INO3-II → Zn+II(NO3)2-II + Ag0
- Zmiany stopni utlenienia: Zn (0 → +II) – utlenianie (oddaje 2 elektrony), Ag (+I → 0) – redukcja (przyjmuje 1 elektron)
- Stosunek elektronów: 2 elektrony oddane / 1 elektron przyjęty. Aby wyrównać elektrony, na 1 atom Zn przypadać muszą 2 atomy Ag.
- Współczynniki: Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
- Sprawdzenie: Równanie jest zbilansowane.
Zbilansowane równanie: Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
Przykład bardziej złożonej reakcji (bilansowanie metodą jonowo-elektronową w środowisku kwasowym):
Niezbilansowane równanie: KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
Po zbilansowaniu (proces pomijamy dla zwięzłości, ale można go prześledzić krok po kroku metodą jonowo-elektronową):
Zbilansowane równanie: 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Częste błędy przy bilansowaniu reakcji redoks
Podczas bilansowania reakcji redoks, zwłaszcza na początku nauki, można popełnić pewne błędy. Do najczęstszych należą:
- Błędne określenie stopni utlenienia. Niewłaściwe przypisanie stopni utlenienia prowadzi do błędnego bilansu elektronowego. Należy dokładnie znać zasady określania stopni utlenienia.
- Niezrozumienie, co to jest utlenianie i redukcja. Pamiętaj: utlenianie to oddawanie elektronów (wzrost stopnia utlenienia), redukcja to przyjmowanie elektronów (spadek stopnia utlenienia).
- Brak uwzględnienia ładunku jonów. Bilansowanie ładunku jest równie ważne jak bilansowanie atomów. Suma ładunków po obu stronach równania musi być równa.
- Błędy w rachunkach matematycznych. Nieprecyzyjne obliczenia zmian stopni utlenienia i ustalanie współczynników mogą prowadzić do błędów.
- Brak sprawdzenia zbilansowanego równania. Zawsze po zbilansowaniu równania należy sprawdzić, czy liczba atomów każdego pierwiastka i ładunek są zbilansowane.
Znaczenie bilansowania reakcji redoks w praktyce
Umiejętność bilansowania reakcji redoks ma szerokie zastosowanie w wielu dziedzinach:
- Chemia analityczna: W analizie ilościowej, np. w miareczkowaniu redoksometrycznym, precyzyjne zbilansowanie reakcji jest kluczowe do obliczenia stężeń substancji.
- Chemia przemysłowa: Wiele procesów przemysłowych, takich jak produkcja metali, nawozów, czy chemikaliów, opiera się na reakcjach redoks. Optymalizacja tych procesów wymaga zrozumienia i bilansowania reakcji.
- Ochrona środowiska: Reakcje redoks odgrywają rolę w procesach oczyszczania wody i powietrza, np. usuwanie zanieczyszczeń przez utlenianie.
- Biochemia: Procesy metaboliczne w organizmach żywych, takie jak oddychanie komórkowe i fotosynteza, to złożone reakcje redoks. Zrozumienie tych reakcji jest niezbędne w biologii i medycynie.
- Elektrochemia: Działanie ogniw galwanicznych i elektrolizerów opiera się na reakcjach redoks. Bilansowanie reakcji jest niezbędne do projektowania i analizy urządzeń elektrochemicznych.
Najczęściej zadawane pytania (FAQ)
- Czy redukcja to oddawanie elektronów?
- Nie, redukcja to przyjmowanie elektronów. Oddawanie elektronów to proces utleniania.
- Jaka jest różnica między utleniaczem a reduktorem?
- Utleniacz to substancja, która przyjmuje elektrony (ulega redukcji) i powoduje utlenienie innej substancji. Reduktor to substancja, która oddaje elektrony (ulega utlenieniu) i powoduje redukcję innej substancji.
- Czy zawsze muszę bilansować reakcje redoks?
- Tak, bilansowanie reakcji redoks jest konieczne, aby równanie reakcji było poprawne i zgodne z prawami chemicznymi. Zbilansowane równanie odzwierciedla rzeczywisty przebieg reakcji i pozwala na poprawne obliczenia stechiometryczne.
- Która metoda bilansowania jest lepsza: stopni utlenienia czy jonowo-elektronowa?
- Obie metody są poprawne i prowadzą do tego samego rezultatu. Wybór metody zależy od rodzaju reakcji i preferencji. Metoda stopni utlenienia jest często szybsza dla prostych reakcji, a metoda jonowo-elektronowa jest bardziej uniwersalna, zwłaszcza dla reakcji w roztworach wodnych i w środowisku kwasowym lub zasadowym.
- Czy mogę zbilansować reakcję redoks "na oko"?
- W przypadku bardzo prostych reakcji czasami można zbilansować równanie "na oko", ale w większości przypadków jest to ryzykowne i prowadzi do błędów. Zawsze zaleca się stosowanie systematycznych metod bilansowania, takich jak metoda stopni utlenienia lub metoda jonowo-elektronowa, aby mieć pewność, że równanie jest zbilansowane poprawnie.
Podsumowanie
Bilansowanie reakcji utleniania-redukcji jest kluczową umiejętnością w chemii. Zrozumienie zasad utleniania i redukcji, a także opanowanie metod bilansowania, pozwala na poprawne opisywanie i przewidywanie przebiegu reakcji chemicznych. Pamiętaj, że redukcja to przyjmowanie elektronów, a bilansowanie elektronowe jest fundamentalne dla poprawności równania reakcji redoks. Regularna praktyka i rozwiązywanie zadań pomoże Ci stać się mistrzem w bilansowaniu reakcji redoks i otworzy drzwi do głębszego zrozumienia chemii.
Jeśli chcesz poznać inne artykuły podobne do Bilansowanie Reakcji Redoks: Klucz do Chemii, możesz odwiedzić kategorię Rachunkowość.

