10/06/2024
Reakcje redoks, znane również jako reakcje utlenienia-redukcji, często postrzegane są jako jedne z trudniejszych zagadnień chemii. Wielu uczniów obawia się ich bilansowania, jednak nie wszystkie reakcje redoks są skomplikowane. Nawet prosta reakcja syntezy wody z pierwiastków jest przykładem reakcji redoks, którą łatwo zbilansować. Jednak, gdy mamy do czynienia z bardziej złożonymi reakcjami, takimi jak roztwarzanie miedzi w rozcieńczonym kwasie azotowym (V), bilansowanie staje się wyzwaniem. Na szczęście istnieją metody, które ułatwiają poradzenie sobie z tym zadaniem. Zrozumienie reakcji redoks jest kluczowe nie tylko w chemii szkolnej, ale również w wielu aspektach życia codziennego i przemysłu.

Czym właściwie są reakcje redoks?
Reakcje redoks charakteryzują się transferem elektronów pomiędzy reagującymi substancjami. Mówiąc prościej, w reakcji redoks jedna substancja oddaje elektrony (utlenia się), a druga je przyjmuje (redukuje się). Spójrzmy na przykład reakcji glinu z tlenkiem miedzi(II):
2Al + 3CuO → Al2O3 + 3Cu
Aby zrozumieć, co dzieje się na poziomie elektronowym, przyjrzyjmy się poszczególnym atomom:
- Glin (Al): Przed reakcją glin jest atomem obojętnym. Po reakcji w tlenku glinu (Al2O3) glin występuje jako kation glinu (Al3+). Aby stać się kationem Al3+, atom glinu musiał oddać 3 elektrony. Mówimy, że glin uległ utlenieniu.
- Miedź (Cu): W tlenku miedzi(II) (CuO) miedź występuje jako kation miedzi(II) (Cu2+). Po reakcji miedź występuje w formie metalicznej (Cu), jako atom obojętny. Aby stać się atomem miedzi, kation Cu2+ musiał przyjąć 2 elektrony. Mówimy, że miedź uległa redukcji.
Podsumowując, glin oddał elektrony, a miedź je przyjęła. To właśnie jest istota reakcji redoks – przeniesienie elektronów z jednego reagenta na drugi.
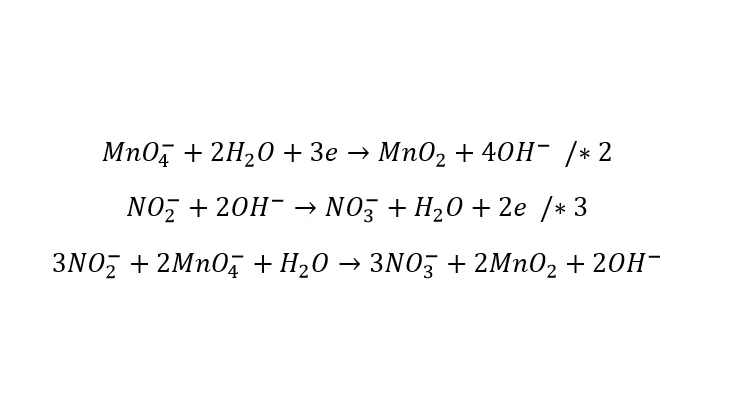
Dlaczego bilansowanie reakcji redoks bywa trudne?
Trudność w bilansowaniu reakcji redoks często wynika z faktu, że zmiany stopni utlenienia (o których więcej powiemy w przyszłości) nie są od razu widoczne na pierwszy rzut oka. W prostych reakcjach, takich jak synteza wody (2H2 + O2 → 2H2O), bilansowanie jest intuicyjne i szybkie. Jednak w bardziej złożonych reakcjach, gdzie wiele pierwiastków zmienia stopnie utlenienia i powstaje kilka produktów, metoda prób i błędów, choć czasami skuteczna, staje się bardzo czasochłonna i frustrująca. Przykładem takiej reakcji jest wspomniane wcześniej roztwarzanie miedzi w rozcieńczonym kwasie azotowym (V):
Cu + HNO3 → Cu(NO3)2 + NO + H2O
Spróbujmy zbilansować tę reakcję metodą prób i błędów, tak jak zostało to opisane w dostarczonym tekście. Zaczynamy od pierwiastków, które występują tylko raz po obu stronach równania – w tym przypadku jest to miedź (Cu). Możemy założyć, że miedź jest już zbilansowana i wstawić współczynniki stechiometryczne równe 1 przy Cu i Cu(NO3)2:
1Cu + HNO3 → 1Cu(NO3)2 + NO + H2O
Teraz spróbujmy zbilansować wodór (H). Po lewej stronie mamy go w kwasie azotowym (HNO3), a po prawej w wodzie (H2O). Początkowo moglibyśmy pomyśleć o współczynnikach 2 przed HNO3 i 1 przed H2O. Jednak szybko zauważymy, że to zaburzy bilans azotu (N).
Po wielu próbach i korektach, metodą prób i błędów, możemy dojść do prawidłowo zbilansowanego równania:
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Jednak, jak widzimy, dojście do tego wyniku wymagało sporo czasu i cierpliwości. Metoda prób i błędów nie jest efektywna w przypadku bardziej skomplikowanych reakcji redoks i łatwo można popełnić błąd.

Znaczenie reakcji redoks w życiu codziennym i przemyśle
Pomimo trudności w bilansowaniu, reakcje redoks są niezwykle ważne i wszechobecne. Odgrywają kluczową rolę w wielu procesach biologicznych, przemysłowych i technologicznych. Oto kilka przykładów:
- Procesy metaboliczne: Oddychanie komórkowe, fotosynteza – to tylko niektóre z fundamentalnych procesów biologicznych opartych na reakcjach redoks.
- Produkcja energii: Spalanie paliw, działanie baterii i ogniw paliwowych – wszystko to opiera się na kontrolowanych reakcjach redoks, w których energia chemiczna przekształcana jest w energię elektryczną lub cieplną. Baterie są modelowymi przykładami procesów redoks.
- Korozja metali: Rdzewienie żelaza, patynowanie miedzi – to niepożądane, ale naturalne procesy redoks, w których metale ulegają utlenianiu pod wpływem czynników środowiskowych. Korozja samochodów jest typowym przykładem reakcji redoks związanej z żelazem.
- Przemysł chemiczny: Wiele procesów przemysłowych, takich jak produkcja nawozów, tworzyw sztucznych, leków i wielu innych substancji, wykorzystuje reakcje redoks na różnych etapach.
- Analiza chemiczna: Reakcje redoks są wykorzystywane w analizie chemicznej, na przykład w miareczkowaniu redoksometrycznym, które pozwala na oznaczanie stężenia substancji utleniających lub redukujących. Pomiar stężenia alkoholu we krwi za pomocą alkomatów opiera się na reakcji redoks etanolu ze związkiem chromu.
- Kosmetyka: Rozjaśnianie włosów za pomocą nadtlenku wodoru to również przykład reakcji redoks.
Czy istnieje łatwiejszy sposób na bilansowanie reakcji redoks?
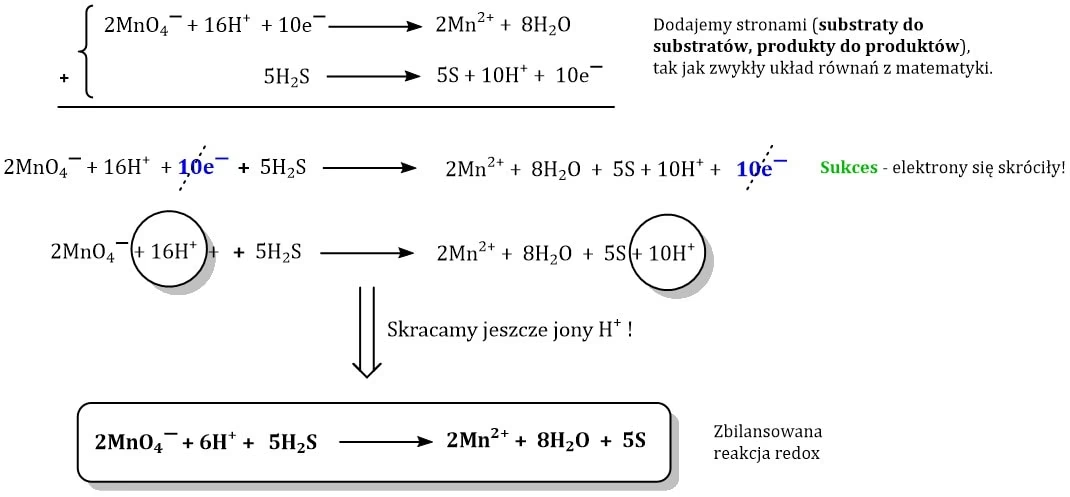
Na szczęście tak! Metoda prób i błędów jest nieefektywna i czasochłonna. Istnieją systematyczne metody bilansowania reakcji redoks, które znacznie ułatwiają to zadanie. Jedną z najpopularniejszych metod jest metoda bilansu elektronowego (metoda jonowo-elektronowa), która bazuje na pojęciu stopni utlenienia i bilansowaniu elektronów oddawanych i przyjmowanych w reakcji. W kolejnych artykułach szczegółowo omówimy tę metodę i pokażemy, jak skutecznie i szybko bilansować nawet najbardziej skomplikowane reakcje redoks. Zrozumienie stopni utlenienia jest kluczowe dla opanowania tej metody.
Najczęściej zadawane pytania (FAQ)
- Co to są reakcje redoks?
- Reakcje redoks to reakcje utlenienia-redukcji, w których następuje transfer elektronów pomiędzy reagującymi substancjami. Jedna substancja oddaje elektrony (utlenia się), a druga je przyjmuje (redukuje się).
- Dlaczego reakcje redoks są ważne?
- Reakcje redoks są fundamentalne dla wielu procesów biologicznych, przemysłowych i technologicznych. Uczestniczą w produkcji energii, korozji metali, procesach metabolicznych, przemysle chemicznym i wielu innych dziedzinach.
- Czy wszystkie reakcje chemiczne to reakcje redoks?
- Nie, nie wszystkie reakcje chemiczne są reakcjami redoks. Istnieją reakcje, w których nie dochodzi do zmiany stopni utlenienia pierwiastków, na przykład reakcje kwasowo-zasadowe lub reakcje strącania osadów.
- Czy istnieje łatwiejszy sposób na bilansowanie reakcji redoks niż metoda prób i błędów?
- Tak, istnieje systematyczna metoda bilansu elektronowego (metoda jonowo-elektronowa), która pozwala na efektywne i szybkie bilansowanie reakcji redoks. Metoda ta zostanie omówiona w kolejnych artykułach.
Podsumowując, reakcje redoks, choć początkowo mogą wydawać się trudne do bilansowania, są niezwykle istotne i powszechne. Zrozumienie ich mechanizmu i opanowanie skutecznych metod bilansowania jest kluczowe dla każdego, kto chce zgłębić tajniki chemii. W kolejnych artykułach przybliżymy systematyczne metody bilansowania, które pozwolą Ci stać się mistrzem reakcji redoks!
Jeśli chcesz poznać inne artykuły podobne do Jak skutecznie bilansować reakcje redoks?, możesz odwiedzić kategorię Rachunkowość.