08/05/2025
Reakcje utleniania i redukcji, znane również jako reakcje redoks, często sprawiają trudności uczniom i studentom chemii. Zrozumienie wymiany elektronów i prawidłowe zbilansowanie równań reakcji redoks może być wyzwaniem. Na szczęście istnieje uniwersalna metoda, która ułatwia to zadanie – bilans jonowo-elektronowy, znany również jako metoda równań połówkowych. W tym artykule przyjrzymy się bliżej tej metodzie, krok po kroku omawiając jej zastosowanie i zalety.

Czym jest bilans jonowo-elektronowy?
Bilans jonowo-elektronowy, inaczej metoda równań połówkowych, to technika bilansowania reakcji redoks poprzez rozdzielenie całej reakcji na dwa półreakcje: reakcję utleniania i reakcję redukcji. Każda półreakcja opisuje proces oddawania lub przyjmowania elektronów przez dany reagent. Metoda ta koncentruje się na bilansowaniu ładunku elektrycznego i atomów w każdej półreakcji oddzielnie, a następnie łączeniu ich w zbilansowane równanie reakcji redoks.
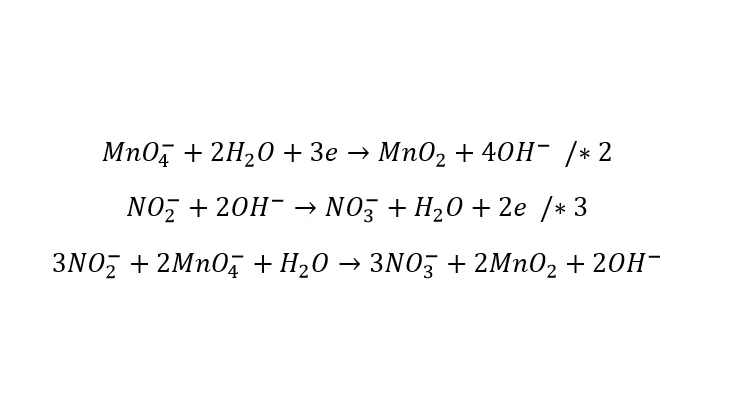
W przeciwieństwie do tradycyjnej metody bilansu elektronowego, która opiera się na bilansowaniu liczby oddanych i przyjętych elektronów w całym równaniu, metoda jonowo-elektronowa skupia się na równaniach połówkowych, które odzwierciedlają rzeczywiste procesy utleniania i redukcji zachodzące na poziomie jonowym. To podejście jest szczególnie przydatne, gdy nie znamy pełnego schematu reakcji, a jedynie obserwujemy pewne zmiany, na przykład zmianę barwy roztworu.
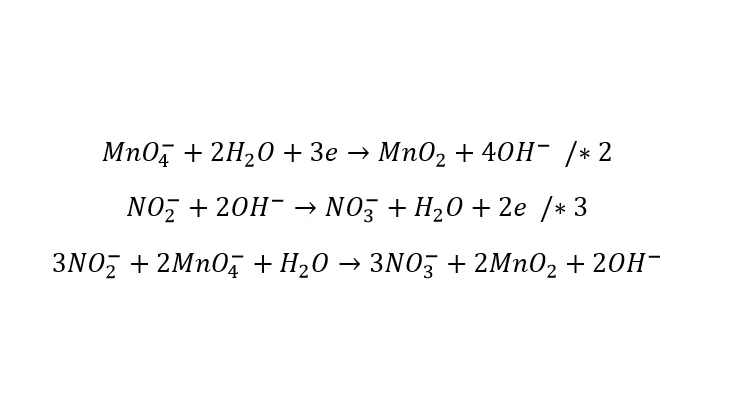
Równania połówkowe a równania cząstkowe
Warto zaznaczyć różnicę pomiędzy równaniami połówkowymi (jonowo-elektronowymi) a równaniami cząstkowymi, stosowanymi w tradycyjnym bilansie elektronowym. Równania cząstkowe, choć prowadzą do poprawnego zbilansowania reakcji pod względem atomów i ładunku, nie są pełnymi równaniami reakcji utleniania i redukcji. Opisują jedynie zmiany stopni utlenienia wybranych atomów, pomijając często udział innych jonów lub cząsteczek w procesie. Z kolei równania połówkowe, po zsumowaniu, dają pełne, zbilansowane równanie reakcji redoks, uwzględniające wszystkie reagenty i produkty.
Krok po kroku: bilans jonowo-elektronowy w praktyce
Metoda bilansu jonowo-elektronowego składa się z kilku prostych kroków, które można zastosować do zbilansowania praktycznie każdej reakcji redoks, niezależnie od środowiska reakcji (kwasowe, zasadowe, obojętne). Poniżej przedstawiamy uniwersalny dekalog bilansowania reakcji redoks metodą jonowo-elektronową:
- Rozdziel reakcję redoks na dwie reakcje połówkowe: utleniania i redukcji. Zidentyfikuj substancje, które ulegają utlenieniu (zwiększenie stopnia utlenienia) i redukcji (zmniejszenie stopnia utlenienia).
- Zbilansuj atomy, które ulegają utlenieniu/redukcji w każdej półreakcji. Czasami konieczne jest dodanie współczynników stechiometrycznych przed wzorami substancji.
- Zbilansuj atomy tlenu, dodając cząsteczki wody (H2O) po stronie, gdzie brakuje atomów tlenu.
- Zbilansuj atomy wodoru, dodając jony wodorowe (H+) po stronie, gdzie brakuje atomów wodoru.
- Zbilansuj ładunek elektryczny w każdej półreakcji, dodając elektrony (e-) po stronie bardziej dodatniej (lub mniej ujemnej).
- Wyrównaj liczbę elektronów w obu półreakcjach, mnożąc każdą półreakcję przez odpowiedni współczynnik. Liczba elektronów oddawanych w reakcji utleniania musi być równa liczbie elektronów przyjmowanych w reakcji redukcji.
- Dodaj do siebie obie półreakcje, sumując substraty z substratami i produkty z produktami. Elektrony powinny się skrócić (zredukować).
- (Środowisko zasadowe) Jeśli reakcja zachodzi w środowisku zasadowym, do każdego jonu H+, który pojawił się w zsumowanym równaniu, dodaj tyle samo jonów wodorotlenkowych (OH-) po obu stronach równania.
- (Środowisko zasadowe) Połącz jony H+ i OH- po jednej stronie równania w cząsteczki wody (H2O) i poskracaj cząsteczki wody, które pojawiają się po obu stronach równania.
- Sprawdź zbilansowanie równania: upewnij się, że liczba atomów każdego pierwiastka i sumaryczny ładunek elektryczny są takie same po obu stronach równania.
Przykłady bilansowania reakcji redoks
Aby lepiej zrozumieć metodę bilansu jonowo-elektronowego, przeanalizujmy kilka przykładów reakcji redoks w różnych środowiskach.

Reakcja w środowisku kwasowym: dichromian(VI) potasu i jony żelaza(II)
Zbilansujmy reakcję:
Cr2O72− + Fe2+ + H+ → Cr3+ + Fe3+ + H2O
- Półreakcje:
- Redukcja: Cr2O72− → Cr3+
- Utlenianie: Fe2+ → Fe3+
- Bilans atomów Cr i Fe:
- Cr2O72− → 2Cr3+
- Fe2+ → Fe3+
- Bilans atomów tlenu:
- Cr2O72− → 2Cr3+ + 7H2O
- Fe2+ → Fe3+
- Bilans atomów wodoru:
- Cr2O72− + 14H+ → 2Cr3+ + 7H2O
- Fe2+ → Fe3+
- Bilans ładunku elektrycznego:
- Cr2O72− + 14H+ + 6e− → 2Cr3+ + 7H2O
- Fe2+ → Fe3+ + 1e−
- Wyrównanie liczby elektronów:
- (Cr2O72− + 14H+ + 6e− → 2Cr3+ + 7H2O) × 1
- (Fe2+ → Fe3+ + 1e−) × 6
- Sumowanie półreakcji:
Cr2O72− + 14H+ + 6e− + 6Fe2+ → 2Cr3+ + 7H2O + 6Fe3+ + 6e−
Po skróceniu elektronów:
Cr2O72− + 14H+ + 6Fe2+ → 2Cr3+ + 7H2O + 6Fe3+
- Krok 8 i 9 pomijamy, ponieważ reakcja zachodzi w środowisku kwasowym.
- Sprawdzenie: Liczba atomów i ładunek są zbilansowane.
Reakcja w środowisku zasadowym: manganian(VII) potasu i azotyn sodu
Zbilansujmy reakcję:
MnO4− + NO2− + OH− → MnO42− + NO3− + H2O
- Półreakcje:
- Redukcja: MnO4− → MnO42−
- Utlenianie: NO2− → NO3−
- Bilans atomów Mn i N:
- MnO4− → MnO42−
- NO2− → NO3−
- Bilans atomów tlenu:
- MnO4− → MnO42−
- NO2− + H2O → NO3−
- Bilans atomów wodoru:
- MnO4− → MnO42−
- NO2− + H2O → NO3− + 2H+
- Bilans ładunku elektrycznego:
- MnO4− + e− → MnO42−
- NO2− + H2O → NO3− + 2H+ + 2e−
- Wyrównanie liczby elektronów:
- (MnO4− + e− → MnO42−) × 2
- (NO2− + H2O → NO3− + 2H+ + 2e−) × 1
- Sumowanie półreakcji:
2MnO4− + 2e− + NO2− + H2O → 2MnO42− + NO3− + 2H+ + 2e−
Po skróceniu elektronów:
2MnO4− + NO2− + H2O → 2MnO42− + NO3− + 2H+
- Dodanie jonów OH-:
2MnO4− + NO2− + H2O + 2OH− → 2MnO42− + NO3− + 2H+ + 2OH−
- Utworzenie wody i skrócenie:
2MnO4− + NO2− + H2O + 2OH− → 2MnO42− + NO3− + 2H2O
Po skróceniu wody:
2MnO4− + NO2− + 2OH− → 2MnO42− + NO3− + H2O
- Sprawdzenie: Liczba atomów i ładunek są zbilansowane.
Pytania i odpowiedzi
Czy reakcje redoks są trudne?
Reakcje redoks mogą wydawać się trudne na początku, ale z odpowiednim podejściem i praktyką stają się łatwiejsze do zrozumienia i bilansowania. Metoda bilansu jonowo-elektronowego jest uniwersalna i systematyczna, co znacznie ułatwia rozwiązywanie zadań z reakcji redoks.
Czy metoda bilansu jonowo-elektronowego jest uniwersalna?
Tak, metoda bilansu jonowo-elektronowego jest uniwersalna i może być stosowana do bilansowania praktycznie wszystkich reakcji redoks, niezależnie od ich złożoności i środowiska reakcji. Jest to potężne narzędzie, które pomaga w zrozumieniu mechanizmów reakcji utleniania i redukcji.

Jakie są zalety metody bilansu jonowo-elektronowego?
Metoda bilansu jonowo-elektronowego ma kilka zalet:
- Systematyczność: Kroki metody są jasno określone i łatwe do śledzenia.
- Uniwersalność: Metoda działa w każdym środowisku reakcji.
- Zrozumienie mechanizmu: Metoda opiera się na rzeczywistych procesach utleniania i redukcji, co pomaga w zrozumieniu, co dzieje się na poziomie jonowym.
- Przydatność w niepełnych danych: Metoda jest szczególnie przydatna, gdy nie znamy pełnego równania reakcji, a jedynie obserwujemy pewne zmiany.
Podsumowanie
Bilans jonowo-elektronowy to skuteczna i uniwersalna metoda bilansowania reakcji redoks. Rozdzielenie reakcji na półreakcje utleniania i redukcji, a następnie systematyczne bilansowanie atomów i ładunku w każdej z nich, prowadzi do poprawnego zbilansowania całego równania reakcji. Metoda ta jest szczególnie przydatna dla osób, które chcą głębiej zrozumieć mechanizmy reakcji redoks i szukają skutecznego narzędzia do rozwiązywania zadań z chemii. Zachęcamy do praktyki i stosowania metody bilansu jonowo-elektronowego, aby reakcje redoks przestały być trudne i stały się zrozumiałe i przewidywalne.
Jeśli chcesz poznać inne artykuły podobne do Bilans jonowo-elektronowy: prosty sposób na reakcje redoks, możesz odwiedzić kategorię Rachunkowość.

