23/04/2023
Wiosenne słońce przyjemnie ogrzewa powietrze, a termometr pokazuje +5°C. Mimo to, na jeziorze wciąż leży gruba warstwa lodu. Dlaczego ta lodowa pokrywa nie znika natychmiast, gdy tylko temperatura przekroczy magiczne 0°C? Odpowiedź kryje się w fascynującym pojęciu fizyki – cieple właściwym.

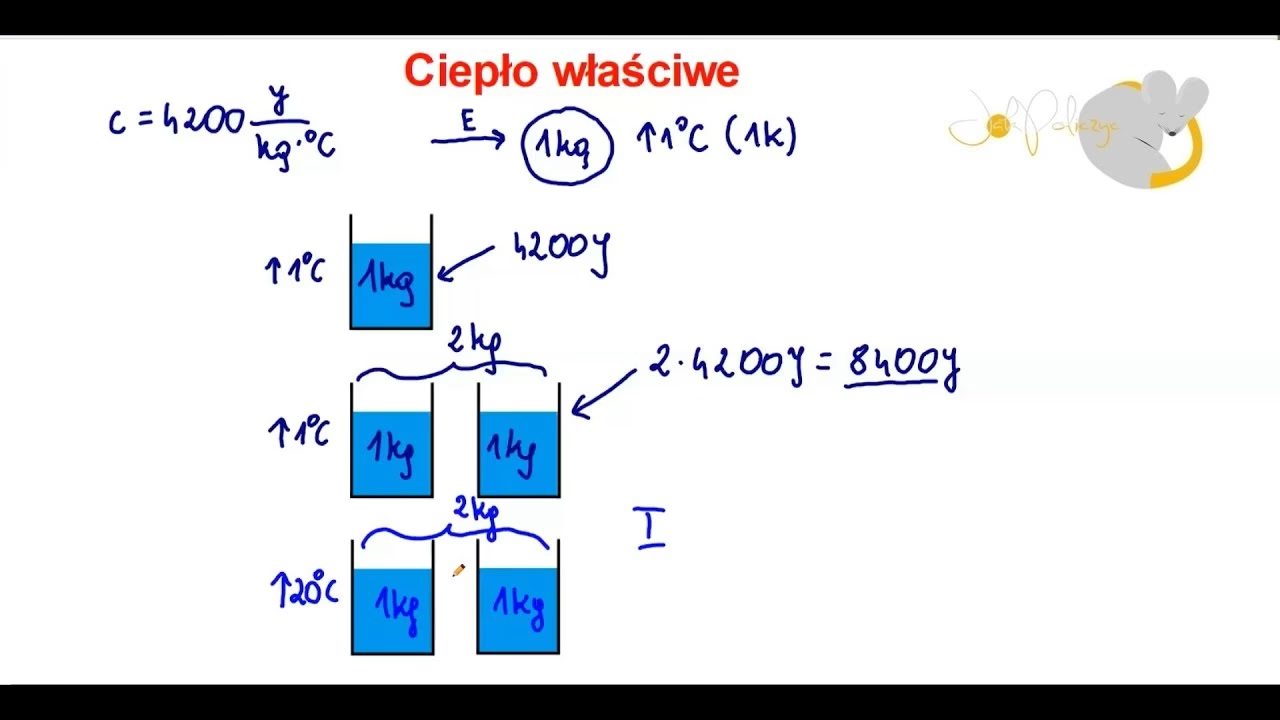
Czym jest ciepło właściwe?
Ciepło właściwe to ilość energii cieplnej, jaką musimy dostarczyć do 1 kilograma danej substancji, aby podnieść jej temperaturę o 1 stopień Celsjusza (lub 1 kelwin). Jest to fundamentalna właściwość każdej substancji, która mówi nam, jak łatwo lub trudno jest zmienić jej temperaturę. Im wyższe ciepło właściwe, tym więcej energii potrzeba, aby ją ogrzać.
Matematycznie, ciepło właściwe (c) definiujemy wzorem:
c = Q / (m · ΔT)
Gdzie:
- c – ciepło właściwe [J/(kg·K)]
- Q – dostarczona energia cieplna (ciepło) [J]
- m – masa ciała [kg]
- ΔT – przyrost temperatury [K lub °C]
Jednostką ciepła właściwego w układzie SI jest dżul na kilogram razy kelwin (J/(kg·K)).
Doświadczenie 1: Jak różne substancje reagują na ciepło?
Aby lepiej zrozumieć pojęcie ciepła właściwego, przeprowadźmy prosty eksperyment.
Materiały:
- Kuchenka elektryczna
- Termometr (0-50°C)
- Waga
- Stoper
- Dwa identyczne naczynia metalowe (ok. 750 ml) z pokrywkami
- Mieszadełko
- Statyw (opcjonalnie)
- Woda
- Olej jadalny
Instrukcja:
- Zważ 250 g wody i umieść w naczyniu. Zmierz temperaturę początkową.
- Umieść naczynie na kuchence i włącz stoper. Zmierz czas potrzebny do podniesienia temperatury wody o 10°C i 20°C.
- Powtórz kroki 1 i 2 z 500 g wody.
- Powtórz kroki 1 i 2 z 500 g oleju.
Wyniki:
Zauważysz, że czas potrzebny do ogrzania wody o 10°C i 20°C różni się w zależności od masy wody i rodzaju substancji (woda vs. olej).
Podsumowanie doświadczenia: Ilość energii potrzebnej do ogrzania substancji zależy od:
- Przyrostu temperatury: Im większy przyrost temperatury, tym więcej energii potrzebujemy.
- Masy substancji: Im większa masa, tym więcej energii jest potrzebne do ogrzania o tę samą temperaturę.
- Rodzaju substancji: Różne substancje mają różne ciepła właściwe.
Dla przykładu, woda ma znacznie wyższe ciepło właściwe niż olej. Oznacza to, że aby ogrzać taką samą masę wody i oleju o tę samą temperaturę, musimy dostarczyć znacznie więcej energii wodzie.
Ciepło właściwe wybranych substancji
Poniższa tabela przedstawia wartości ciepła właściwego dla różnych substancji:
| Substancja stała | Ciepło właściwe [J/(kg·K)] | Substancja ciekła | Ciepło właściwe [J/(kg·K)] | Gaz | Ciepło właściwe [J/(kg·K)] |
|---|---|---|---|---|---|
| Ołów | 130 | Rtęć | 140 | Metan | 1854 |
| Szkło | 700 | Nafta | 2210 | Dwutlenek węgla | 654 |
| Miedź | 380 | Benzyna | 2090 | Powietrze | 729 |
| Złoto | 130 | Gliceryna | 2430 | Hel | 3140 |
| Lód | 2090 | Woda | 4180 | Para wodna | 1380 |
| Beton | 920 | Eter | 2340 | Tlen | 649 |
Przykłady obliczeń
Przykład 1: Ogrzewanie betonowej kostki
O ile wzrośnie temperatura betonowej kostki o masie 3,7 kg, jeśli dostarczymy jej 6808 J energii?
Korzystając ze wzoru ΔT = Q / (c · m), gdzie c dla betonu wynosi 920 J/(kg·K):
ΔT = 6808 J / (920 J/(kg·K) · 3,7 kg) = 2 K = 2°C
Temperatura kostki wzrośnie o 2 stopnie Celsjusza.
Przykład 2: Ogrzewanie powietrza w pokoju
Ile ciepła trzeba dostarczyć, aby ogrzać powietrze w pokoju o objętości 50 m³ o 10°C? Gęstość powietrza wynosi 1,3 kg/m³, a ciepło właściwe 729 J/(kg·K).
Najpierw obliczamy masę powietrza: m = d · V = 1,3 kg/m³ · 50 m³ = 65 kg.
Następnie obliczamy potrzebne ciepło: Q = c · m · ΔT = 729 J/(kg·K) · 65 kg · 10 K = 473 850 J.
Aby ogrzać powietrze w pokoju o 10°C, potrzeba około 474 kJ energii.

Ciepło topnienia i krzepnięcia
Dostarczanie ciepła nie zawsze powoduje wzrost temperatury. Podczas zmiany stanu skupienia, na przykład podczas topnienia lodu lub wrzenia wody, dostarczana energia jest wykorzystywana na zmianę struktury substancji, a nie na podnoszenie temperatury.
Ciepło topnienia (krzepnięcia) to ilość energii, jaką należy dostarczyć (odebrać), aby stopić (zestalić) 1 kilogram substancji w stałej temperaturze. Jednostką jest J/kg.
Wzór na ciepło topnienia: L = Q / m
Doświadczenie 2: Topnienie lodu
Umieść pokruszony lód w naczyniu z termometrem. Mimo dostarczania ciepła z otoczenia, temperatura mieszaniny lodu z wodą pozostanie stała (0°C) do czasu, aż cały lód się stopi. Energia jest zużywana na zmianę stanu skupienia lodu w wodę.
Ciepło parowania i skraplania
Podobnie, podczas wrzenia cieczy, dostarczana energia jest wykorzystywana na zmianę stanu skupienia cieczy w gaz, a temperatura pozostaje stała.

Ciepło parowania (skraplania) to ilość energii, jaką należy dostarczyć (odebrać), aby odparować (skroplić) 1 kilogram substancji w danej temperaturze. Jednostką jest J/kg.
Wzór na ciepło parowania: R = Q / m
Doświadczenie 3: Wrzenie wody
Umieść naczynie z wodą na kuchence i doprowadź do wrzenia. Temperatura wody podczas wrzenia pozostanie stała (ok. 100°C), mimo ciągłego dostarczania ciepła. Energia jest zużywana na zmianę stanu skupienia wody w parę wodną.
Dlaczego lód nie topi się od razu?
Wracając do pytania ze wstępu: lód na jeziorze nie topi się natychmiast, ponieważ proces topnienia wymaga dostarczenia dużej ilości energii – ciepła topnienia. Nawet jeśli temperatura powietrza jest powyżej 0°C, energia cieplna z otoczenia musi być dostarczona do lodu, aby nastąpiło topnienie. Proces ten jest stopniowy i zależy od ilości dostarczanej energii i masy lodu.
Pytania i odpowiedzi (FAQ)
- Jak definiuje się ciepło właściwe?
- Ciepło właściwe to ilość energii cieplnej potrzebna do ogrzania 1 kilograma substancji o 1 stopień Celsjusza.
- O czym mówi ciepło właściwe?
- Ciepło właściwe mówi o tym, jak trudno jest zmienić temperaturę danej substancji. Substancje o wysokim cieple właściwym trudniej ogrzać i ochłodzić.
- Ile wynosi ciepło właściwe drewna?
- Ciepło właściwe drewna zależy od rodzaju drewna i jego wilgotności, ale zazwyczaj mieści się w zakresie 1700-2500 J/(kg·K).
Podsumowanie
Ciepło właściwe, ciepło topnienia i ciepło parowania to kluczowe pojęcia do zrozumienia wymiany ciepła i zmian stanów skupienia materii. Ciepło właściwe charakteryzuje, jak łatwo zmienić temperaturę substancji, natomiast ciepło topnienia i parowania opisują energię potrzebną do zmiany stanu skupienia. Zrozumienie tych pojęć pozwala wyjaśnić zjawiska takie jak powolne topnienie lodu wiosną czy stabilna temperatura wrzenia wody.
Jeśli chcesz poznać inne artykuły podobne do Ciepło właściwe: klucz do zrozumienia wymiany ciepła, możesz odwiedzić kategorię Rachunkowość.