28/04/2024
W branżach farmaceutycznej i wyrobów medycznych, audyty dostawców stanowią nieodzowny element zapewnienia jakości i bezpieczeństwa produktów. Agencje regulacyjne, takie jak FDA, wymagają od producentów przeprowadzania zarówno audytów wewnętrznych, jak i audytów dostawców, aby upewnić się, że przestrzegane są Dobre Praktyki Wytwarzania (GMP) oraz normy ISO. Te audyty są kluczowe w identyfikacji potencjalnych problemów, które mogłyby negatywnie wpłynąć na jakość, skuteczność lub bezpieczeństwo produktów, a także stanowią mechanizm wdrażania działań naprawczych minimalizujących ryzyko dla zdrowia publicznego.
- Kto przeprowadza audyty dostawców i dlaczego są one tak ważne?
- Oczekiwania regulacyjne dotyczące zarządzania jakością dostawców
- Audyty wewnętrzne a audyty dostawców
- Rodzaje audytów dostawców
- Kiedy przeprowadzać audyty dostawców?
- Obszary audytu dostawców
- Wyzwania w audytach dostawców
- Najlepsze praktyki w radzeniu sobie z wyzwaniami audytu dostawców
- Ustanowienie solidnego programu audytu dostawców
- Podsumowanie
- Często zadawane pytania (FAQ)
Kto przeprowadza audyty dostawców i dlaczego są one tak ważne?
Odpowiedzialność za jakość i zgodność produktów spoczywa na producentach, nawet jeśli korzystają oni z usług zewnętrznych dostawców. Często błędne jest przekonanie, że outsourcing zwalnia producenta z odpowiedzialności regulacyjnej. W rzeczywistości, to producent ponosi ostateczną odpowiedzialność za produkty wprowadzane na rynek. Dlatego monitorowanie i zarządzanie jakością w całym łańcuchu dostaw jest absolutnie kluczowe.
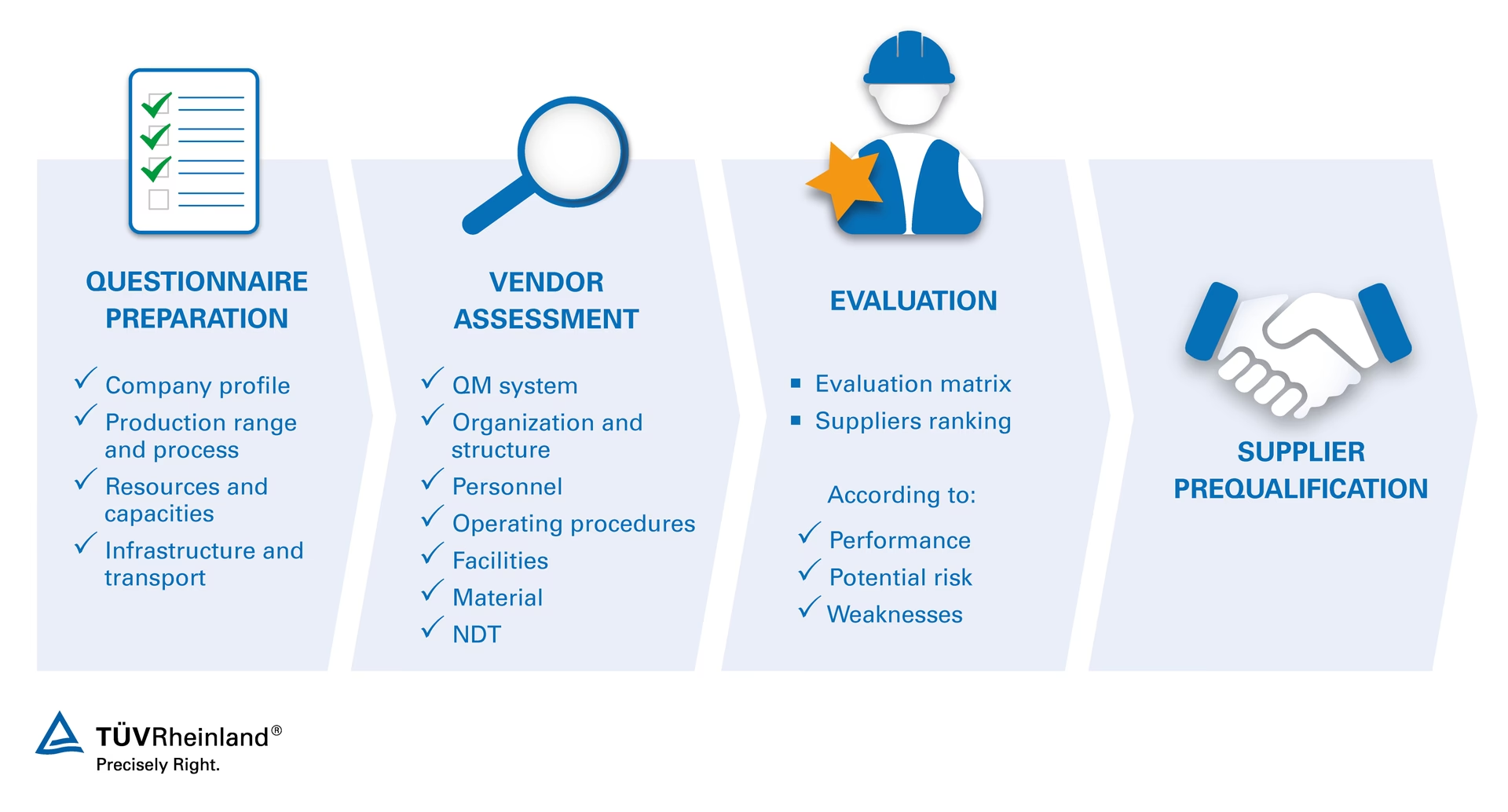
Audyty dostawców są niezbędne, aby upewnić się, że dostawcy, kontraktorzy i konsultanci spełniają określone wymagania jakościowe i regulacyjne. Pomagają one zidentyfikować potencjalne słabości w systemach jakości dostawców, zanim te problemy wpłyną na produkt końcowy. Dzięki audytom producenci mogą podejmować proaktywne działania w celu minimalizacji ryzyka i zapewnienia ciągłości dostaw wysokiej jakości komponentów i usług.
Oczekiwania regulacyjne dotyczące zarządzania jakością dostawców
Zarówno w branży farmaceutycznej, jak i wyrobów medycznych, istnieją jasne wytyczne regulacyjne dotyczące zarządzania jakością dostawców. W sektorze farmaceutycznym kluczowe jest wytyczne Q10 Pharmaceutical Quality System Guidance, które podkreśla odpowiedzialność zleceniodawcy za ocenę kompetencji i zdolności zleceniobiorcy do wykonania powierzonego zadania. Wszystkie ustalenia dotyczące jakości powinny być jasno określone w pisemnej umowie.
W przypadku wyrobów medycznych, regulacje 21 CFR Part 820, a konkretnie sekcja 820.50 dotycząca kontroli zakupów, nakładają na producentów obowiązek opracowania i utrzymywania procedur zapewniających, że wszystkie zakupione produkty i usługi spełniają określone wymagania jakościowe. Regulacje te wymagają od producentów:
- Oceny i selekcji potencjalnych dostawców na podstawie ich zdolności do spełnienia wymagań jakościowych.
- Określenia rodzaju i zakresu kontroli nad dostawcami, w zależności od wyników oceny.
- Prowadzenia rejestru zatwierdzonych dostawców.
Kluczowe jest zrozumienie terminu „ustanowić” w kontekście regulacji FDA. Zgodnie z 21 CFR Part 820.3, „ustanowić” oznacza zdefiniowanie, udokumentowanie i wdrożenie. W kontekście kontroli zakupów, dokładna dokumentacja jest absolutnie niezbędna.
Audyty wewnętrzne a audyty dostawców
Chociaż oba rodzaje audytów są istotne dla zapewnienia jakości, różnią się one zakresem i celem.

| Audyt Wewnętrzny | Audyt Dostawcy |
|---|---|
| Ocena własnych procesów i zgodności z GMP i innymi standardami regulacyjnymi. | Obiektywna ocena procesów dostawcy i zgodności z wymaganiami regulacyjnymi. |
| Element systemu zarządzania jakością producenta. | Kluczowy element zapewnienia jakości zakupionych produktów i usług. |
| Identyfikacja potencjalnych problemów i wdrażanie działań naprawczych wewnątrz firmy. | Identyfikacja potencjalnych problemów związanych z zakupionymi produktami i usługami, które mogą wpłynąć na produkcję wewnętrzną. |
| Dążenie do ciągłego doskonalenia procesów wewnętrznych. | Zapewnienie jakości i zgodności produktów i usług dostarczanych przez zewnętrznych partnerów. |
Rodzaje audytów dostawców
Firmy regulowane przez FDA przeprowadzają różne rodzaje audytów dostawców, aby zapewnić zgodność z przepisami i utrzymać jakość i bezpieczeństwo produktów. Często różne typy audytów są łączone w zależności od potrzeb.
- Audyty Systemu Jakości (Quality System Audits): Oceniają system zarządzania jakością dostawcy pod kątem zgodności z normami FDA, w tym kontrolę projektu, produkcję, testowanie produktów i zapewnienie jakości.
- Kontrole przed zatwierdzeniem (Pre-Approval Inspections - PAI): Dla firm farmaceutycznych, audyty PAI przeprowadzane są u dostawców substancji czynnych (API) lub krytycznych komponentów przed zatwierdzeniem nowej aplikacji leku przez FDA.
- Audyty Dobrej Praktyki Wytwarzania (Good Manufacturing Practice - GMP): Koncentrują się na zgodności dostawcy z regulacjami GMP, kluczowymi dla zapewnienia spójnej produkcji i kontroli produktów zgodnie z normami jakości.
- Audyty Dobrej Praktyki Laboratoryjnej (Good Laboratory Practice - GLP): Dotyczą dostawców przeprowadzających niekliniczne badania laboratoryjne, zapewniając zgodność z regulacjami GLP, które gwarantują jakość i rzetelność danych bezpieczeństwa.
- Audyty Dobrej Praktyki Klinicznej (Good Clinical Practice - GCP): Dla dostawców zaangażowanych w badania kliniczne, audyty GCP oceniają zgodność z regulacjami zapewniającymi rzetelność danych badań klinicznych i ochronę uczestników badań.
- Audyty Bezpieczeństwa Łańcucha Dostaw (Supply Chain Security Audits): Oceniają bezpieczeństwo łańcucha dostaw dostawcy, w tym transport i przechowywanie, aby zapobiec zanieczyszczeniu, fałszowaniu lub innym naruszeniom integralności produktu.
- Audyty Integralności Danych (Data Integrity Audits): Koncentrują się na dokładności i wiarygodności danych dostawcy, w tym praktykach prowadzenia dokumentacji, przechowywania danych i systemach przetwarzania danych.
- Audyty oparte na ryzyku (Risk-Based Audits): Dostosowane do profilu ryzyka dostawcy i krytyczności dostarczanych materiałów lub usług, mogą obejmować kombinację powyższych obszarów w zależności od zidentyfikowanych ryzyk.
Kiedy przeprowadzać audyty dostawców?
Producent regulowany przez FDA powinien przeprowadzać audyty dostawców w kilku kluczowych momentach i w różnych okolicznościach, aby zapewnić zgodność i utrzymać jakość i bezpieczeństwo swoich produktów.
- Przed nawiązaniem współpracy z nowym dostawcą: Audyt inicjujący jest kluczowy do oceny zdolności dostawcy do spełnienia wymagań regulacyjnych i jakościowych.
- Okresowe audyty planowe: Przeprowadzane regularnie, często corocznie lub co dwa lata, aby zapewnić ciągłą zgodność i zidentyfikować zmiany w procesach lub systemach jakości dostawcy.
- W przypadku istotnych zmian: Zmiany w operacjach dostawcy, zarządzaniu, procesach produkcyjnych lub materiałach mogą wymagać nowego audytu.
- Po rozwiązaniu problemu: Audyt kontrolny po wdrożeniu działań naprawczych, aby upewnić się, że problemy zostały odpowiednio rozwiązane.
- Częstotliwość oparta na ryzyku: Dostawcy wysokiego ryzyka lub dostarczający krytyczne komponenty mogą wymagać częstszych audytów.
- Zmiany wymagań regulacyjnych: Zmiany w przepisach FDA lub normach branżowych mogą wymagać audytu w celu zapewnienia zgodności z nowymi wymaganiami.
- Audyty losowe lub niezapowiedziane: Dają dokładniejszy obraz typowych operacji dostawcy i stanu zgodności.
- Skargi rynkowe lub konsumenckie: W przypadku skarg lub zdarzeń niepożądanych związanych z jakością lub bezpieczeństwem produktów.
- Jako element ciągłego doskonalenia: Audyty mogą być częścią programu ciągłego doskonalenia jakości, efektywności i zgodności w łańcuchu dostaw.
- W przypadku pojawienia się trendów lub problemów w branży: Audyt w celu zapewnienia, że dostawca skutecznie radzi sobie z szerszymi wyzwaniami.
Obszary audytu dostawców
Audyt dostawców dla producenta regulowanego przez FDA obejmuje kilka kluczowych obszarów, aby zapewnić zgodność z normami regulacyjnymi i utrzymać jakość i bezpieczeństwo produktu.
- System Zarządzania Jakością (QMS): Ocena zgodności z normami branżowymi i wymaganiami regulacyjnymi, w tym dokumentacja, procedury i zapisy.
- Dobra Praktyka Wytwarzania (GMP): Ocena przestrzegania przepisów GMP, w tym czystość, konserwacja sprzętu, szkolenie personelu i kontrola procesów.
- Zgodność z przepisami: Weryfikacja zgodności z przepisami FDA i innymi obowiązującymi wymogami regulacyjnymi.
- Jakość i specyfikacje produktu: Zapewnienie, że dostarczane produkty lub materiały spełniają uzgodnione specyfikacje i standardy jakości.
- Kontrola i walidacja procesów: Ocena kontroli procesów dostawcy i procedur walidacyjnych, aby zapewnić spójność i niezawodność produkcji.
- Kwalifikacja i wydajność dostawcy: Przegląd procesu kwalifikacji dostawcy i dotychczasowej wydajności, w tym terminowości dostaw i standardów jakości.
- Kontrola zmian (Change Control): Ocena procedur kontroli zmian dostawcy, zapewniających dokumentowanie, ocenę i komunikację wszelkich zmian w materiałach, procesach lub sprzęcie.
- Działania korygujące i zapobiegawcze (CAPA): Przegląd systemu CAPA dostawcy, zapewniającego skuteczną identyfikację, dokumentowanie i rozwiązywanie problemów jakościowych.
- Integralność danych i prowadzenie dokumentacji: Ocena integralności i dokładności danych dostawcy oraz praktyk prowadzenia dokumentacji.
- Identyfikowalność łańcucha dostaw i materiałów: Ocena identyfikowalności materiałów w całym łańcuchu dostaw.
- Kontrola środowiska: Ocena kontroli środowiskowych dostawcy, w tym temperatury, wilgotności i kontroli zanieczyszczeń.
- Szkolenie i kompetencje pracowników: Przegląd programów szkoleniowych i kompetencji personelu dostawcy.
- Obiekty i sprzęt: Inspekcja obiektów i sprzętu dostawcy pod kątem odpowiedniości i utrzymania.
- Zarządzanie ryzykiem: Ocena praktyk zarządzania ryzykiem dostawcy i sposobów identyfikacji, oceny i łagodzenia potencjalnych ryzyk.
- Zarządzanie poddostawcami: Ocena zarządzania poddostawcami przez dostawcę.
- Skargi i opinie klientów: Przegląd sposobu, w jaki dostawca rozpatruje skargi i opinie klientów.
- Historia audytów i inspekcji: Przegląd historii audytów i inspekcji dostawcy.
Ponadto, wykwalifikowany audytor może ocenić zdolność dostawcy do skalowalności produkcji, cyberbezpieczeństwo, oraz odporność łańcucha dostaw.
Wyzwania w audytach dostawców
Liderzy jakości odpowiedzialni za audyty dostawców w branżach regulowanych przez FDA napotykają szereg wyzwań:
- Złożone łańcuchy dostaw: Wielość poziomów dostawców w różnych krajach utrudnia utrzymanie widoczności i kontroli standardów jakości.
- Ocena ryzyka i priorytetyzacja: Skuteczna ocena i priorytetyzacja ryzyk wśród różnych dostawców.
- Różnice geograficzne i kulturowe: Różnice w przepisach, językach i praktykach kulturowych.
- Ograniczenia zasobów: Ograniczony czas, budżet i personel.
- Opór dostawcy lub brak współpracy: Opór przed audytami lub brak pełnej współpracy.
- Integralność danych i przejrzystość: Zapewnienie integralności i przejrzystości danych dostarczanych przez dostawców.
- Zróżnicowanie dojrzałości dostawców: Różnice w dojrzałości jakościowej, możliwościach technologicznych i zrozumieniu wymagań regulacyjnych.
Najlepsze praktyki w radzeniu sobie z wyzwaniami audytu dostawców
- Mapowanie łańcucha dostaw: Opracowanie szczegółowej mapy łańcucha dostaw, identyfikującej każdego dostawcę i przepływ materiałów.
- Macierz ryzyka: Opracowanie wielowymiarowej macierzy ryzyka, oceniającej dostawców na podstawie różnych czynników.
- Lokalni audytorzy: Zatrudnianie lub współpraca z audytorami posiadającymi lokalną wiedzę.
- Partnerstwo z firmą audytorską: Współpraca z renomowaną firmą audytorską w celu uzyskania dostępu do wykwalifikowanych audytorów.
- Jasna komunikacja: Jasne komunikowanie celów, zakresu i korzyści audytu dostawcom.
- Weryfikacja danych: Wdrażanie rygorystycznych procesów weryfikacji danych dostawców.
- Programy rozwoju dostawców: Wdrażanie programów rozwoju dostawców, pomagających im spełnić standardy jakości.
Ustanowienie solidnego programu audytu dostawców
Ustanowienie solidnego programu audytu dostawców obejmuje kilka kluczowych kroków:
- Zdefiniowanie celów i zakresu: Określenie celów programu audytu i zakresu audytowanych dostawców i procesów.
- Opracowanie kryteriów i standardów audytu: Opracowanie jasnych kryteriów audytu na podstawie wymagań regulacyjnych i standardów branżowych.
- Zasoby dla zespołu audytowego: Zapewnienie dostępu do wykwalifikowanych audytorów z odpowiednią wiedzą i doświadczeniem.
- Planowanie i harmonogramowanie audytów: Priorytetyzacja audytów na podstawie oceny ryzyka i komunikacja z dostawcami w celu ustalenia harmonogramu.
- Przeprowadzanie audytów i raportowanie wyników: Dokładna ocena oparta na kryteriach i listach kontrolnych, gromadzenie dowodów i kompilacja kompleksowych raportów.
- Działania następcze i korygujące: Współpraca z dostawcami w celu opracowania planów działań korygujących i monitorowanie ich wdrażania.
- Przegląd i ciągłe doskonalenie: Analiza wyników audytu w czasie w celu identyfikacji trendów i obszarów do poprawy, oraz regularna aktualizacja programu audytu.
- Dokumentacja i prowadzenie rejestrów: Prowadzenie szczegółowej dokumentacji wszystkich audytów, raportów i działań korygujących.
Podsumowanie
Audyty dostawców są nieodzownym elementem zapewnienia jakości i zgodności w branżach regulowanych. Solidny program audytu dostawców, uwzględniający kluczowe obszary, rodzaje audytów, wyzwania i najlepsze praktyki, pomaga producentom minimalizować ryzyko, budować silne relacje z dostawcami i gwarantować bezpieczeństwo i skuteczność produktów dla pacjentów.
Często zadawane pytania (FAQ)
- Kto jest odpowiedzialny za przeprowadzanie audytów dostawców?
- Zazwyczaj audyty dostawców przeprowadzają zespoły ds. jakości producenta lub zewnętrzne firmy audytorskie.
- Jak często należy przeprowadzać audyty dostawców?
- Częstotliwość audytów zależy od profilu ryzyka dostawcy i krytyczności dostarczanych produktów lub usług, zazwyczaj od corocznych do rzadszych audytów w przypadku dostawców o niskim ryzyku.
- Co się dzieje, jeśli audyt dostawcy ujawni niezgodności?
- Producent współpracuje z dostawcą w celu opracowania i wdrożenia planu działań korygujących w celu usunięcia niezgodności.
- Czy audyty dostawców są obowiązkowe?
- Tak, w branżach regulowanych, takich jak farmaceutyczna i wyrobów medycznych, audyty dostawców są wymagane przez agencje regulacyjne w celu zapewnienia zgodności z GMP i innymi standardami.
Jeśli chcesz poznać inne artykuły podobne do Audyty dostawców: klucz do jakości i zgodności, możesz odwiedzić kategorię Audyt.